DISSEMINAZIONE
-
Avvicinare l’EBM alla realtà clinicaIl mondo quotidiano della clinica spesso non si avvale, come potrebbe, delle novità proposte dalle evidenze pubblicate sulle maggiori riviste...
-
Scrivere di BIAS
Quanto uno studio potrebbe sbagliarsiAvresti mai immaginato di scrivere un articolo scientifico sui bias negli studi clinici? Proprio sulla RoB2 (risk of bias2), e... -
Concluso il corso su revisioni sistematiche e meta-analisiSi è conclusa la terza edizione del corso di perfezionamento che dal 2016 l’Università di Milano dedica alle revisioni sistematiche...
-
Unimi, quattro anni di formazione metodologica in ricerca clinicaSi è aperta il 12 febbraio presso il Dipartimento di Scienze Biomediche per la Salute la nuova edizione del corso...
-
EBM in Accademia, la formazione che mancavaAccademia ed EBM sono universi spesso distanti. Uno studente di medicina può concludere il proprio percorso di studi senza quasi...
Key Point
Key points della domanda di ricerca
Differenza tra domanda di background e foreground
La domanda di background, o di fondo, ricerca risposte generali su una malattia, un trattamento, un esame e si configura attraverso domande quali: Chi? Che cosa? Dove? Quando? Come? Perché?
La domanda di foreground, o di primo piano, ricerca risposte specifiche per prendere decisioni cliniche e ha 4 componenti essenziali:
- Paziente e/o problema
- Intervento e/o esposizione
- Confronto, se esiste
- Outcome (esito clinico)
Al formato PICO possono essere aggiunte anche le lettere T e S, diventando PICO(T)(S).
La T è il tempo in cui verrà valutato l’esito e la S lo study design ovvero la tipologia di disegni di studio che si decide di includere nella ricerca.
Da dove nascono le domande di ricerca?
- Da un gap conoscitivo
- Dalla pratica clinica quotidiana
- Dalle discussioni con colleghi e pazienti
- In fase di preparazione di studi, revisioni sistematiche e linee guida
Le domande di ricerca rispondono a due criteri: la rilevanza e l’incertezza
- Rilevanza, quale domanda è più importante per la salute del paziente?
- Incertezza, quale domanda ricorre nella vostra pratica professionale?
Le tipologie di quesiti clinici riguardano domande inerenti:
- La Terapia
- La Prevenzione
- La Diagnosi
- La Prognosi
- L’ Eziologia
Scegliere la domanda che…
- È più importante per il benessere del paziente
- È più pertinente per la vostra necessità di conoscenza
- Alla quale potreste rispondere con il tempo che avete a disposizione
- È più interessante per voi
- Ricorre più frequentemente nella vostra pratica professionale
“One-third of a trial’s time between the germ of your idea and its publication in the New England Journal of Medicine should be spent fighting about the research question”
David L. Sackett
Key points del protocollo di ricerca
Cos’è il protocollo di ricerca
- Rappresenta la mappa per orientarsi circa la conduzione di uno studio
- Nel mondo degli studi clinici e delle revisioni sistematiche è la base per la registrazione degli stessi (ad esempio Clinicaltrials.gov o Prospero)
- Riporta l’ipotesi di ricerca (obiettivi), i metodi (disegno e metodologia), le considerazioni statistiche principali, l’organizzazione dello studio, i contatti dei ricercatori
È importante perché
Consente di sapere quali studi sono in corso, riducendo eventuali duplicazioni e permettendo un maggior coordinamento degli sforzi di ricerca.
Permette di valutare eventuali discrepanze tra ciò che viene programmato nel protocollo e ciò che viene effettivamente fatto durante lo studio (reporting bias).
Troppe indicazioni, quali seguire?
Esistono diverse linee guida che suggeriscono come deve essere sviluppato un protocollo di ricerca.
Per gli studi clinici una di queste guide molto apprezzabile è lo SPIRIT Statement¹’²
Standard Protocol Items: Recommendations for Interventional Trials
- Dettaglia raccomandazioni evidence-based sui contenuti essenziali che ogni protocollo dovrebbe includere
- Le raccomandazioni sono delineate all’interno di una checklist con 33 item
- Promuove la trasparenza della ricerca e dei suoi metodi
- È riconosciuto a livello internazionale come standard di riferimento per la stesura dei protocolli dei trial
Un protocollo di ricerca completo, trasparente e ben scritto facilita la conduzione dello studio e la sua valutazione, nonché la stesura del report finale, attraverso:
- un’accurata valutazione degli aspetti metodologici ed etici della ricerca prima dell’inizio dello studio
- un attento monitoraggio dello studio durante la sua conduzione
¹Chan A-W, Tetzlaff JM, Altman DG, Laupacis A, Gøtzsche PC, Krleža-Jerić K, Hróbjartsson A, Mann H, Dickersin K, Berlin J, Doré C, Parulekar W, Summerskill W, Groves T, Schulz K, Sox H, Rockhold FW, Rennie D, Moher D. SPIRIT 2013 Statement: Defining standard protocol items for clinical trials. Ann Intern Med 2013;158:200-207.
²Chan A-W, Tetzlaff JM, Gøtzsche PC, Altman DG, Mann H, Berlin J, Dickersin K, Hróbjartsson A, Schulz KF, Parulekar WR, Krleža-Jerić K, Laupacis A, Moher D. SPIRIT 2013 Explanation and Elaboration: Guidance for protocols of clinical trials. BMJ 2013;346:e7586.
Key points sugli outcome clinici
Gli outcome clinici sono parte integrante del quesito clinico
Gli outcome o endpoint sono le “misure di esito”, ossia le misurazioni che sono state eseguite per rispondere al quesito dello studio. A seconda della direzione, grandezza e significatività statistica dell’outcome primario si decide se lo studio è positivo, non conclusivo o negativo…
Le domande da farsi in partenza…
- Cosa vorrei misurare?
- Come effettuo la misurazione?
- Quando?
Tipologie di outcome
- Dicotomico o qualitativo, ad es: presenza/assenza dello stato patologico, sesso f/m, fumo si/no.
- Continuo o quantitativo, ad es: pressione arteriosa; peso corporeo, può assumere uno spettro continuo di valori in un certo intervallo.
- Tempo all’evento, ad es. sopravvivenza libera dalla progressione di malattia; rappresenta il tempo trascorso fino al verificarsi (o meno) di un evento.
Outcome “hard” e “soft”
- Outcome “hard”: sono determinati in modo inequivocabile ed oggettivo, ad es. la mortalità, n° di giorni di ricovero.
- Outcome “soft”: la loro determinazione è dipendente dall’operatore o dal paziente, ad es. il miglioramento/peggioramento della qualità di vita, del dolore o di sintomi. Possono essere influenzati da imprecisioni, valutazioni soggettive o dalla conoscenza del trattamento somministrato.
Gerarchia degli outcome
- Primario: è quello che determina il calcolo del campione e il risultato principale dello studio.
- Secondari: supportano ulteriori analisi a conferma o meno dell’outcome primario. Possono avere carattere esplorativo.
- Outcome co-primari: più outcome hanno lo stesso livello di importanza e devono essere valutati congiuntamente, ad es: efficacia e sicurezza di un farmaco. A volte richiedono disegni più complessi e un campione numerico più elevato.
- Outcome composito: due o più eventi concorrono allo stesso outcome, ad es. la sopravvivenza libera dalla progressione di malattia, dove si considerano eventi sia la mortalità, sia la progressione di malattia.
- Outcome surrogato: è un indicatore utilizzato per fornire una misura indiretta dell’effetto di un trattamento, e dovrebbe essere predittivo di un outcome clinico rilevante. Per es. la sopravvivenza libera dalla progressione di malattia è un outcome surrogato rispetto alla mortalità. Sono molto utilizzati perché sono più facili da misurare o è richiesto meno tempo perché di verifichino. Ad es. nei pazienti ipertesi, la diminuzione della pressione arteriosa può essere identificata come un outcome surrogato di eventi cardiovascolari maggiori e di una maggiore sopravvivenza; nei diabetici, la diminuzione della glicemia un surrogato di insorgenza di un minor numero di complicanze e di maggiore sopravvivenza.
Key points degli errori sistematici – risk of bias
L’errore casuale e l’errore sistematico
Errore casuale: si verifica per effetto del caso, replicazioni multiple della stessa misurazione producono risultati differenti, in tutte le direzioni per variazioni casuali, ma la media dà il risultato corretto. È misurabile con dei test statistici.
Errore sistematico (bias): si verifica per la presenza di un fattore che distorce sistematicamente le osservazioni nella stessa direzione. Replicazioni multiple della stessa misurazione producono risultati sempre nella stessa direzione e “sbagliati”.
Il bias
Il bias o distorsione sistematica dell'effetto stimato di un intervento, può essere causato da errori nel disegno, nella conduzione di uno studio clinico, nell’analisi e valutazione dei dati, e nella pubblicazione dei risultati.
I risultati di uno studio sono tanto più validi (probabilmente veri) quanto meno sono affetti da errori sistematici (bias).
I bias vanno previsti ed evitati o quantomeno ridotti, fin dalla fase di disegno dello studio.
Una mappa delle tipologie di bias nello sviluppo degli studi randomizzati controllati (RCT)
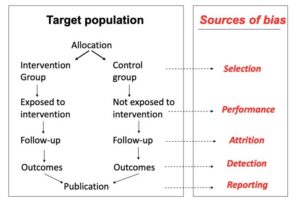
Selection bias
Si verifica quando esistono sbilanciamenti sistematici nelle caratteristiche al basale (prima dell’inizio dello studio) tra il gruppo di intervento e quello di controllo.
Negli studi randomizzati l'assegnazione dei soggetti al trattamento o al controllo avviene in modo casuale per garantire che tutte le variabili prognostiche (note e non note) si distribuiscano in maniera uniforme nel gruppo sperimentale e in quello di controllo.
Se la randomizzazione non è eseguita in maniera corretta è possibile introdurre un bias di selezione anche negli studi randomizzati.
Performance bias
Si realizza quando si verificano delle differenze sistematiche nell’assistenza fornita ai due gruppi di pazienti (trattati e controlli), oltre il trattamento oggetto di sperimentazione.
Ad esempio:
- Diversa frequenza della valutazione, delle visite di controllo, somministrazione di altri trattamenti non previsti dal protocollo.
- Differenze sistematiche nei comportamenti dei partecipanti assegnati ai due gruppi, ad es chi sa di assumere un farmaco anti-ipertensivo potrebbe essere maggiormente motivato ad adottare uno stile di vita più sano e a sottoporsi regolarmente ai controlli, aumentando così le probabilità di guarigione per motivi indipendenti dal trattamento sperimentato.
Si previene con la cecità (blinding) di pazienti e operatori, quando possibile. Esistono casi laddove la cecità non è attuabile, quali ad es. gli interventi psicosociali, educativi, chirurgici, e riabilitativi.
Detection bias
Si realizza quando si verificano delle differenze sistematiche nella modalità in cui l’esito viene valutato e/o individuato.
Ad esempio:
- Se la valutazione dell’outcome è soggettiva, e il paziente non è in cieco, si può suggestionare, generando una forte convinzione a favore del trattamento, e potrebbe quindi percepire un maggiore miglioramento rispetto al paziente che sa di non ricevere il trattamento.
- Se il medico conosce il trattamento che sta ricevendo il suo paziente potrebbe fare delle domande specifiche per rilevare dei benefici o effetti collaterali che si aspetta.
Si previene con la cecità, specialmente di chi “convive” con l’esito, il paziente, e di chi valuta l’esito, ovvero dell’“outcome assessor”, che può essere il medico che somministra il trattamento, o una terza persona.
Attrition bias
Si verifica quando il numero totale di soggetti che abbandonano prematuramente lo studio è elevato (ad es per interruzione del trattamento o perdita al follow up). Spesso l’abbandono non è omogeneo tra i bracci, realizzandosi quindi uno sbilanciamento nel numero di soggetti che rimangono nello studio. In questo caso i due gruppi di confronto (trattati e controlli) non sono più sovrapponibili.
Il bias si verifica quando c’è un’associazione tra le ragioni per le quali i pazienti escono da uno studio e l’intervento in esame. Queste ragioni possono essere varie, come il mancato beneficio o rilevanti effetti collaterali.
Reporting bias
Si verifica quando nella pubblicazione dei risultati di uno studio vengono riportati solo una parte degli esiti misurati o solo alcune delle misure utilizzate per rilevare l’esito, preferendo quindi alcune informazioni a altre, in modo similare alla propaganda. Più spesso gli autori riportano gli esiti (o le misure) con risultati statisticamente significativi o favorevoli.





